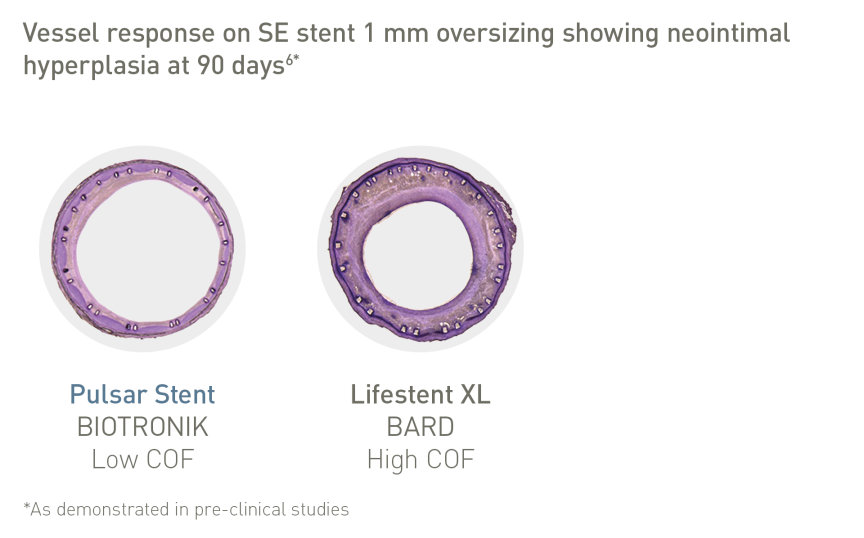
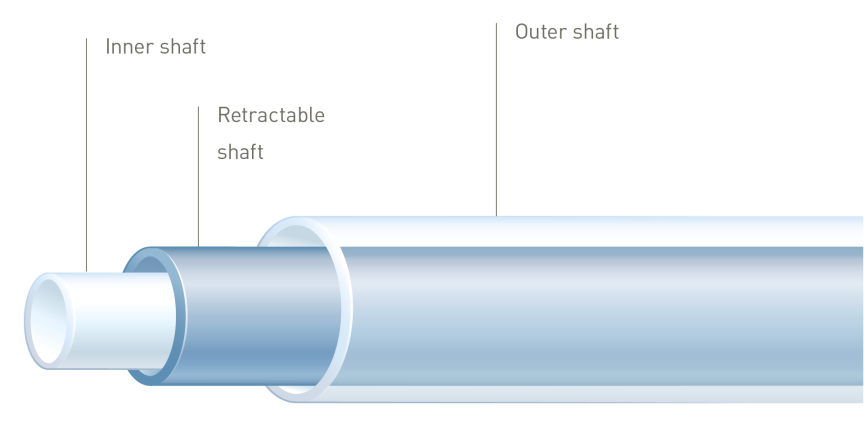
Cieńsze przęsła sprawiają, że siła wywierana stale na ścianę naczynia (COF) jest mniejsza²
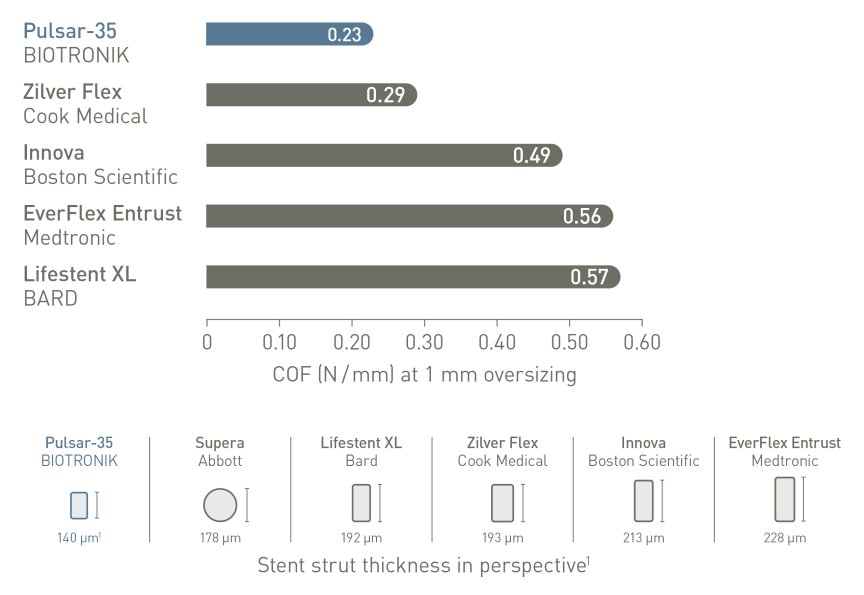
Cieńsze przęsła i mniejsza siła wywierana na ścianę naczynia (COF) mają znaczenie*:
• Niższe ryzyko restenozy3
• Mniej uszkodzeń i stanów zapalnych w naczyniach3
• Szybsza endotelializacja4,5