Amvia Edge DR-T/SR-T
O sistema de estimulação do Amvia Edge oferece-lhe opções. Usufrua de mais opções de tratamento, incluindo estimulação fisiológica e ferramentas para atuar contra o desenvolvimento de fibrilação atrial (FA).
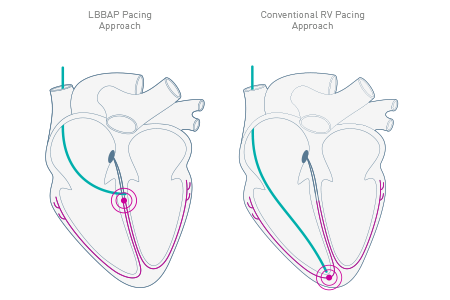
Como o primeiro pacemaker aprovado para a abordagem de estimulação da área do ramo esquerdo (LBBAP, left-bundle branch area pacing)1, o Amvia Edge promove padrões naturais de contração do miocárdio aos seus pacientes. Proporciona frequências cardíacas fisiológicas com estimulação em malha fechada (CLS) e visa manter o ritmo sinusal com ATP atrial (aATP).
Ao mesmo tempo, o Amvia Edge automatiza diversas tarefas rotineiras durante fluxos de trabalho de implante, avaliação em consultório, monitoramento remoto e RM. Ofereça a estimulação fisiológica exclusiva aos os seus pacientes, melhore a terapia e economize tempo nos fluxos diários de trabalho para que mais pacientes possam beneficiar de cuidados mais personalizados.
Principais características do produto
Obter a estimulação fisiológica
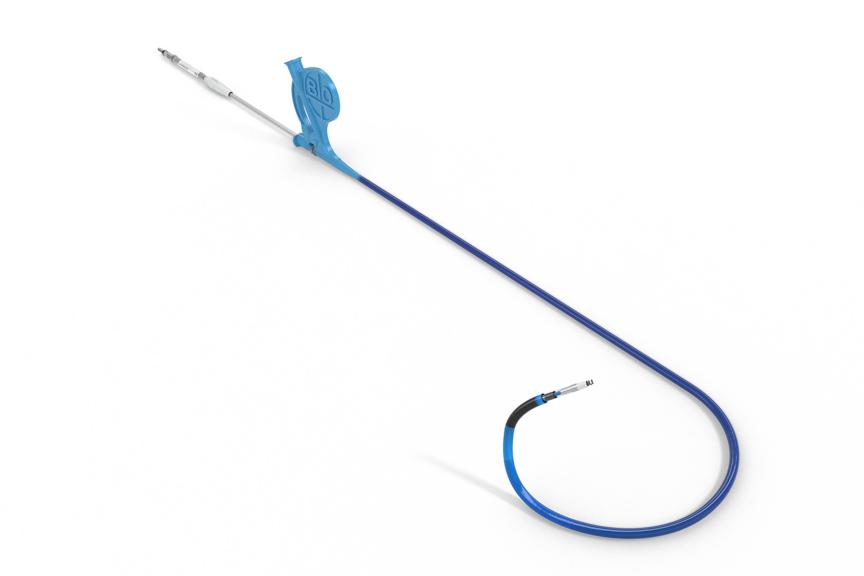
O Amvia Edge é o primeiro pacemaker aprovado para a estimulação da área do ramo esquerdo (LBBAP).1 Além disso, a tecnologia exclusiva do sensor de estimulação em malha fechada (CLS) do Amvia Edge acompanha o sistema nervoso autónomo e adapta-se automaticamente2 para simular a regulação intrínseca natural.3
Gerir arritmias atriais
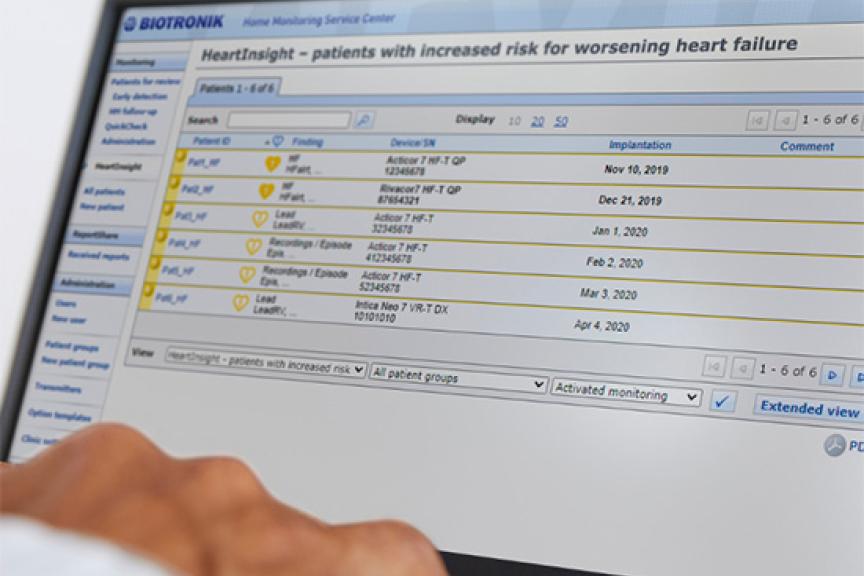
O Amvia Edge visa ajudar os pacientes a manterem as frequências cardíacas fisiológicas ao longo do tempo. Combina as capacidades de monitorização atrial em consultório e remoto com as ferramentas de gestão de arritmia de ATP atrial (aATP) para atuar ativa e precocemente contra o desenvolvimento da fibrilação atrial (FA).14
Simplificar planos de tratamento
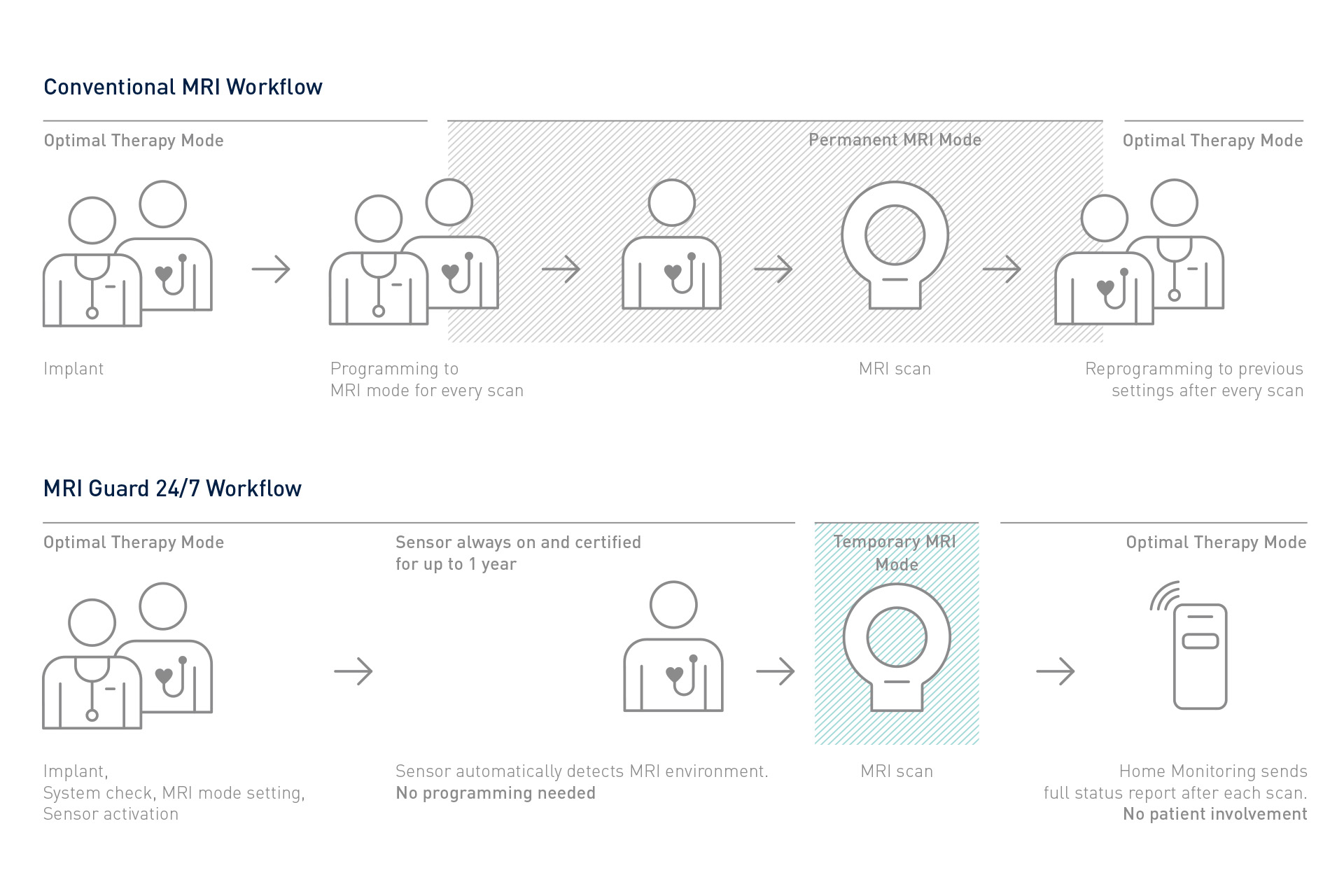
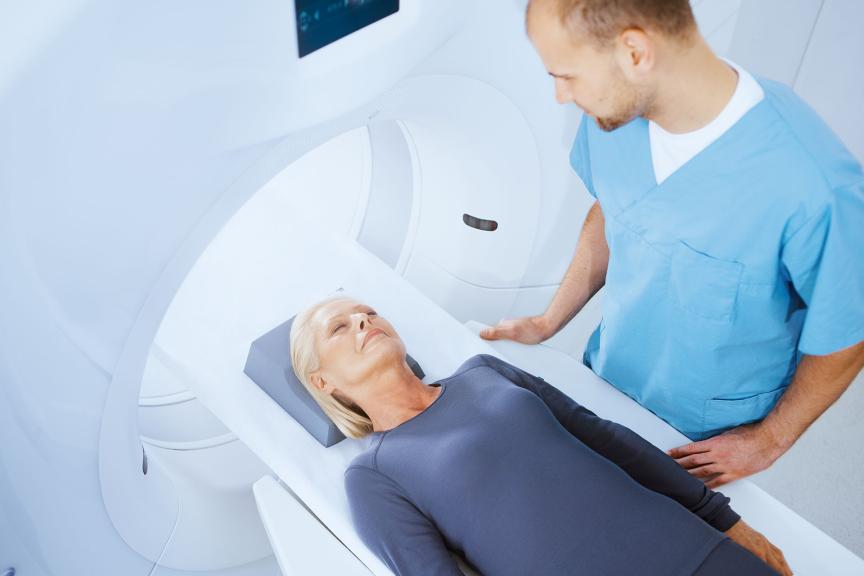
O Amvia Edge inclui diversas soluções que otimizam os fluxos de trabalho ao longo da jornada do paciente, do implante e das avaliações ao monitoramento remoto e acesso excepcional à RM.
Média
Downloads e links relacionados
Contacto
Referências
1) Manual técnico do Amvia Edge da BIOTRONIK, manual do Medtronic Azure XT DR MRI SureScan™; manual técnico do Accolade MRI™ da Boston Scientific; manual do usuário do Assurity MRI™ da Abbott; manual do implante do MicroPort Alizea™. 2) Lindovska M, Kameník L, Pollock B, et al. Clinical observations with Closed Loop Stimulation pacemakers in a large patient cohort: the CYLOS routine documentation registry (RECORD). Europace. 2012; 14: 1587-1595. 3) Santini M, Ricci R, Pignalberi C, et al. Effect of autonomic stressors on rate control in pacemakers using ventricular impedance signal. Pacing Clin Electrophysiol. 2004; 27: 24-32. 4) Sharma PS, Patel NR, Ravi V, et al. Clinical outcomes of left bundle branch area pacing compared to right ventricular pacing: Results from the Geisinger-Rush Conduction System Pacing Registry. Heart Rhythm. 2022; 19(1): 3-11. 5) De Pooter J, Ozpak E, Calle S, et al. Initial experience of left bundle branch area pacing using stylet-driven pacing leads: A multicenter study. J Cardiovasc Electrophysiol. 2022; 33(7): 1540-1549. Exclusão de responsabilidade: Este material apenas resume o uso investigativo de ferramentas para estimulação do sistema de condução (CSP) por De Pooter et al. em seu estudo clínico. Observe que o eletrodo Solia S não é aprovado para CSP. As ferramentas de CSP da BIOTRONIK não estão atualmente aprovadas para a estimulação do sistema de condução nos Estados Unidos. Conteúdo não destinado a prestadores de serviços de saúde nos Estados Unidos. 6) Menezes AS, Daher MT, Nascente CM, Moreira HG, Moreira TAC e Campos RN. Correlation among Closed Loop Stimulation, cardiopulmonary capacity, and quality of life PBMR. 2003; 8(2): 119-124. 7) Pavri BB and Russel S. An impedance sensor is superior to an accelerometer for chronotropically incompetent patients with sinus node dysfunction: results of a pilot study with a dual sensor pacemaker. Circulation. 2006; 114: II_749. 8) Coenen M, Malinowski K, Spitzer W, et al. Closed Loop Stimulation and accelerometer based rate adaptation: results of the PROVIDE study, Europace. 2008; 10: 327-333. 10) Malinowski K. Interindividual comparison of different sensor principles for rate adaptive pacing PACE. 1998; 21(PT II): 2209-2213. 10) Abi-Samra FM, Singh N, Rosin BL, DwyerJV e Miller C. Europace. 2013; 15: 849-856. 11) Puglisi A, Favale S, Scipione P, et al. Overdrive versus conventional closed-loop rate modulation pacing in the prevention of atrial tachyarrhythmias in brady-tachy syndrome: on behalf of the Burden II study group. Pacing Clin Electrophysiol. 2008; 11: 1443-55. 12) Ikeda S, Nogami A, Inoue K, et al. Closed‐loop stimulation as a physiological rate‐modulated pacing approach based on intracardiac impedance to lower the atrial tachyarrhythmia burden in patients with sinus node dysfunction and atrial fibrillation. J Cardiovasc Electrophysiol. 2020; 31: 1187-1194. 13) Coenen M, Malinowski K, Spitz W, et al. Closed loop stimulation and accelerometer-based rate adaptation: results of the PROVIDE study. Europace. 2008; 10: 327-333. 14) Mabo P, Victor F, Bazin P, et al. A randomized trial of long-term remote monitoring of pacemaker recipients (the COMPAS trial). Eur Heart J. 2012; 33(9): 1105-1111. 15) Nattel S, Burstein B, Dobrev D. Atrial remodeling and atrial fibrillation: mechanisms and implications. Circ Arrhythm Electrophysiol. 2008; 1(1): 62-73. 16) Dados em arquivo. 17) Varma N, Epstein AE, Irimpen A, et al. Efficacy and safety of automatic remote monitoring for implantable cardioverter-defibrillator follow-up: the Lumos-T Safely Reduces Routine Office Device Follow-up (TRUST) trial. Circulation. 2010; 122(4): 325-332. 18) Mullane S, Michaelis K, Henrickson C, et al. Utilization and programming of an automatic MRI recognition feature for cardiac rhythm management devices. Heart Rhythm O2. 2021; 2: 132-137. 19). Dados em arquivo. 20) Siddamsetti S, Shinn A, Gautam S. Remote programming of cardiac implantable electronic devices: a novel approach to program cardiac devices for magnetic resonance imaging. J Cardiovasc Electrophysiol. 2022;33(5):1005–1009. 21) Watanabe E, Yamazaki F, Goto T, et al. Remote management of pacemaker patients with biennial in-clinic evaluation: continuous Home Monitoring in the Japanese At-Home study: A randomized clinical trial. Circ Arrhythm Electrophysiol. 2020 May;13(5):e007734. doi: 10.1161/CIRCEP.119.007734. 22) Garcia-Fernández FJ, Asensi JO, Romero R, et al. Safety and efficiency of a common and simplified protocol for pacemaker and defibrillator surveillance based on remote monitoring only: a long-term randomized trial (RM-ALONE). Eur Heart J. 2019; 40(23): 1837-1846. 23) Ricci RP, Morichelli L, Quarta L, et al. Long-term patient acceptance of and satisfaction with implanted device remote monitoring, Europace. 2010; 12(5): 674-679. 24) Dados em arquivo. 25) Dados em arquivo. 26) Amvia Edge SR-T 10 anos; Garantia limitada para dispositivos cardíacos eletrônicos implantáveis da BIOTRONIK; Descrição resumida da garantia limitada da Medtronic; Informações e formulários de garantia limitada da Boston Scientific; Manual de referência dos procedimentos de garantia da Abbott CRM; Manual de implante do MicroPort Alizea DR™/Alizea SR™. 27) Amvia Edge DR-T 8 anos; Garantia limitada para dispositivos cardíacos eletrônicos implantáveis da BIOTRONIK; Descrição resumida da garantia limitada da Medtronic; Informações e formulários de garantia limitada da Boston Scientific; Manual de referência dos procedimentos de garantia da Abbott CRM; Manual de implante do MicroPort Alizea DR™/Alizea SR ™. 28) Amvia Edge SR-T: A 2,5 V/0,4 ms, 60 bpm, 500 Ω; estimulação: 50%, Home Monitoring: OFF, QuickCheck: OFF, telemetria por RF: OFF. 29) Amvia Edge DR-T: A: 2,5 V/0,4 ms, 60 bpm, 500 Ohm; estimulação: 50%, VD: 2,5 V/0,4 ms, 60 bpm, 500 Ohm; estimulação: 5%, Home Monitoring OFF, QuickCheck: OFF, telemetria por RF: OFF, supressão de Vp: ON.